Ein Schweizer, ein Brite und ein gebürtiger Deutscher bekommen für ihre Arbeit auf dem Gebiet der Kryo-Elektronenmikroskopie den Chemie-Nobelpreis. Ihre Erkenntnisse erlauben einen völlig neuen Blick auf die Moleküle des Lebens und helfen bei der Entwicklung besserer Medikamente.
Stuttgart - Ohne Proteine gibt es kein Leben. Die komplexen Biomoleküle sind an praktisch allen Aktivitäten lebender Zellen beteiligt. Sie steuern als Enzyme den Stoffwechsel, beeinflussen als Hormone wichtige Körperfunktionen oder wehren als Antikörper Krankheitserreger ab – und vieles mehr. So wichtig Proteine sind, so schwierig ist es, sie zu erforschen und ihre Struktur aufzuklären, denn die Eiweißmoleküle sind nicht nur sehr klein, sondern auch äußerst empfindlich und komplex.
Der Schweizer Jacques Dubochet, der in Deutschland geborene Amerikaner Joachim Frank und der Brite Richard Henderson haben trotzdem einen Weg gefunden, mit dem sich die Moleküle des Lebens mit immer höherer Präzision, vor allem aber unter realitätsnahen Bedingungen studieren lassen. Für ihre Arbeiten auf dem Gebiet der Kryo-Elektronenmikroskopie haben die drei Forscher jetzt den Chemienobelpreis erhalten. Die Vorsilbe Kryo- rührt daher, dass die Wissenschaftler dabei mit sehr niedrigen Temperaturen arbeiten.
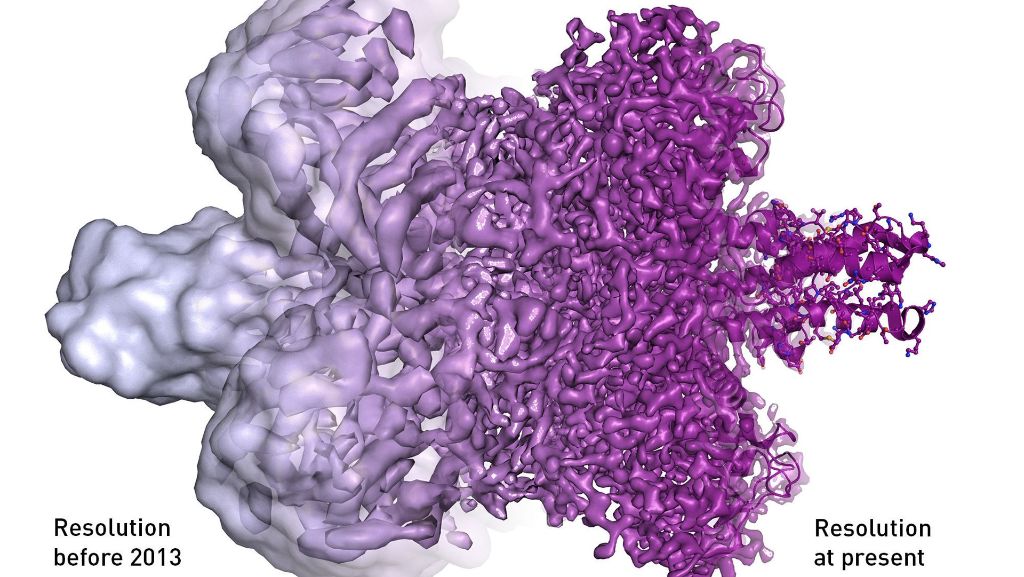
„Diese Methode hat für die Biochemie eine neue Ära begründet“, heißt es in der Begründung des Nobelkomitees. Die Kryo-Elektronenmikroskopie sei nicht nur wichtig für das grundlegende Verständnis der Chemie des Lebens, sondern auch für die Entwicklung neuer Medikamente. So wurde das Zikavirus, das bei Säuglingen zu schweren Hirnschäden führt, mit dieser Technik analysiert. Binnen weniger Monate gelang es so, ein dreidimensionales Bild des Virus zu gewinnen – mit einer Auflösung, bei der sogar einzelne Atome sichtbar werden. Dadurch hätten Wissenschaftler rasch mit der Suche nach möglichen Angriffspunkten für neue Medikamente beginnen können, schreiben die Juroren.
Probleme der Elektronenmikroskopie
Der Weg zur Entwicklung der Kryo-Elektronenmikroskopie war lang. Mit Elektronenmikroskopen können Forscher zwar schon seit den 1930er Jahren sehr kleine Strukturen untersuchen. Allerdings war die Methode zunächst für unbelebte Materie gedacht. Denn biologisches Material wird durch den starken Elektronenstrahl in kürzester Zeit zerstört. Zudem herrscht im Inneren eines Elektronenmikroskops ein Vakuum. Das führt dazu, dass das im Untersuchungsobjekt enthaltene Wasser in kürzester Zeit verdampft – das Präparat trocknet aus.
Das natürliche Medium der Biomoleküle ist aber Wasser. Erst in wässriger Lösung können sich Proteine zu den faszinierenden dreidimensionalen Gebilden auffalten, die das Leben am Laufen halten. Trocknen sie aus, fallen sie zusammen, verlieren ihre natürliche Struktur – und die Aufnahmen sind wertlos. „Biomoleküle machen ihre Arbeit in Wasser“, sagte die Vorsitzende des Nobelkomitees, Sara Snogerup Linse, bei der Preisverleihung – und schüttete demonstrativ den Inhalt eines Laborgefäßes mit einer Proteinlösung in ein Glas Wasser.
Der Schotte Richard Henderson ließ sich nicht von den Problemen der Elektronenmikroskopie entmutigen. Er schuf 1975 das erste 3-D-Modell eines Bakterienproteins. Damit die Proben nicht austrockneten, bedeckte er sie mit einer Glukoselösung. Zudem setzte er schwächere Elektronenstrahlen ein. Allerdings hatte Henderson ein Protein ausgewählt, das in der Zellmembran des Bakteriums fixiert war. Proteine, die in einer Lösung schwimmen, ließen sich so nicht untersuchen. Sie zappeln sozusagen ständig vor der Kamera herum und werden deshalb in ganz unterschiedlichen Positionen von den Elektronenstrahlen erwischt. Anders als viele Skeptiker glaubte Henderson, dass sich auch solche Moleküle mit dem Elektronenmikroskop untersuchen lassen.
Mathematische Modelle
Hier kommt der gebürtige Deutsche Joachim Frank ins Spiel. Er arbeitete seit 1975 an einem mathematischen Modell, mit dem sich aus verschiedenen Blickwinkeln entstandene unscharfe Bilder zu wenigen scharfen Bildern vereinigen lassen. In einem weiteren Schritt setzte er daraus hochauflösende dreidimensionale Bilder zusammen. Die Entwicklung der Algorithmen war 1981 abgeschlossen. „Kryo-Elektronenmikroskopie erweitert das Spektrum der Moleküle, die wir studieren können, beträchtlich“, sagte Frank, der bei der Pressekonferenz per Telefon zugeschaltet war.
Einen weiteren entscheidenden Beitrag zur Perfektionierung der Methode lieferte der Schweizer Jacques Dubochet. Um das Austrocknen unter dem Elektronenmikroskop zu verhindern und Proteine in ihrer natürlichen Form studieren zu können, verpasste er ihnen eine Schutzhülle aus Eis – genauer gesagt: aus sogenanntem vitrifiziertem Eis, das so klar wie Glas ist. Dubochet gelang das 1982 durch die Abkühlung der Proben auf minus 196 Grad mit gekühltem Ethan und flüssigem Stickstoff. Normalerweise würden sich dabei Eiskristalle bilden, die die Elektronenstrahlen in alle Richtungen werfen und scharfe Bilder unmöglich machen. Dubochet verhinderte das durch eine extrem schnelle Abkühlung.
Kryo-Elektronenmikroskopie macht es auch möglich, Proteine in unterschiedlichen Phasen ihrer Aktivität zu beobachten: Hängt man die Einzelbilder hintereinander, entsteht ein Film, aus dem Biochemiker viel lernen können. „Jetzt können wir die Enzyme, die Moleküle des Lebens, in Aktion sehen“, sagte Nobeljuror Peter Somfai. Der Deutsch-Amerikaner Frank bremst allerdings die Hoffnungen auf schnelle praktische Erfolge auf breiter Front – etwa in der Molekularmedizin: „Das ist Grundlagenforschung. Bis zur Anwendung werden noch viele Jahre vergehen“. Juror Peter Brzezinsiki gibt zu bedenken, dass Proteine bislang nicht innerhalb von Zellen untersucht werden können, sondern nur in isolierter Form.
Die Nobelpreisträger für Chemie 2017
Jacques Dubochet „Von optimistischen Eltern gezeugt“ – so steht es im Lebenslauf des 75-jährigen Schweizers Jacques Dubochet. Mit 14 wurde bei dem Biophysiker eine Leseschwäche diagnostiziert: „Das erlaubte mir, schlecht in allem zu sein – und Leute mit Schwierigkeiten zu verstehen“, sagte er später.
Joachim Frank Geboren wurde der Biophysiker Joachim Frank 1940 in Siegen, in München machte er seinen Doktor. Nach einem Aufenthalt in Kalifornien kehrte er 1972 ans Max-Planck-Institut für Biochemie nach Deutschland zurück. Seit 1975 ist er in den USA, nun lehrt er an der Columbia University in New York.
Richard Henderson
Der 1945 in Edinburgh geborene „schottische Bauernsohn“ – wie er sich nennt – ist seit 1973 am molekularbiologischen MRC-Labor im britischen Cambridge. Als Schüler half dem Molekularbiologen und Biophysiker Richard Henderson ein Stipendium. Heute beklagt er die starke Bürokratie.